 © Deutschen Herzstiftung e. V. © MedicalARTWORK
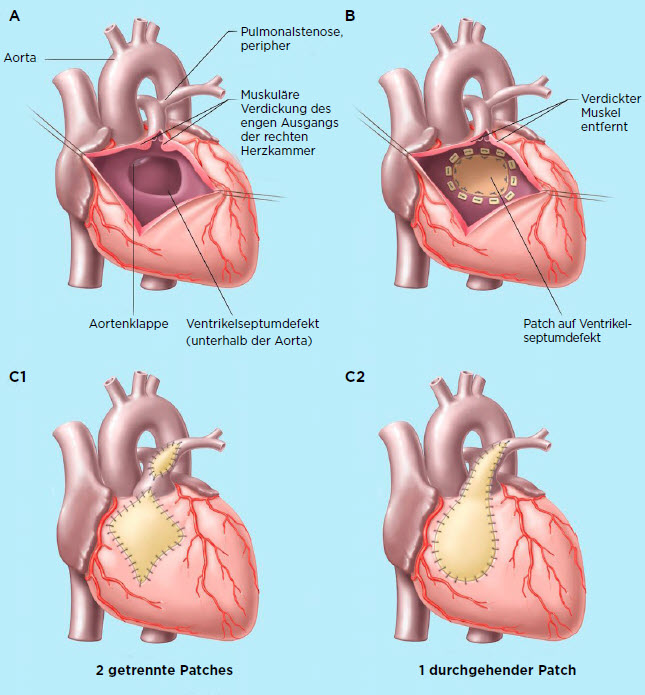
© Deutschen Herzstiftung e. V. © MedicalARTWORKAbb. 3: Fallot´sche Tetralogie vor und nach der operativen Reparatur A: Sicht in das über die rechte Herzkammer geöffnete Herz B: Die Kammerscheidewand ist verschlossen, die verdickte Muskulatur der Ausflussbahn der rechten Kammer ist entfernt C1: Voneinander unabhängige Erweiterung der rechten Kammer und der engen Pulmonalarterie in zwei getrennten Patches. C2: Transannuläre Patcherweiterungsplastik (TAP), durch die der Ring der Pulmonalklappe erweitert und damit eröffnet werden musste
Herzrhythmusstörungen
Supraventrikuläre und ventrikuläre Tachykardien sowie bradykarde Herzrhythmusstörungen gehören besonders bei Patienten mit Vorhofseptumdefekt, Fallot‘scher Tetralogie (Abb. 3), Ebstein‘scher Anomalie, nach Vorhof-umkehr- oder nach Fontan-Operation zu den häufigsten Todesursachen [6, 19-22]. Bei supraventrikulären Tachykardien handelt es sich häufig um intraatriale Re-Entry-Tachykardien oder Vorhofflattern, während Vorhofflimmern bei jüngeren Patienten mit AHF seltener gesehen wird. Wichtig ist, dass bei manchen AHF auch supraventrikuläre Tachykardien oft schlecht toleriert werden und zur Dekompensation oder zum Tod führen, während dies bei Patienten ohne AHF meist nicht der Fall ist. Ventrikuläre Arrhythmien sind vorzugsweise nach Ventrikulotomien, z.B. bei Fallot-Reparatur oder nach anderen komplexen Korrekturoperationen mit Einbringen von Fremdmaterialen (z. B. Rastelli-Opera- tion) zu finden [6, 21].
Die Arrhythmiebehandlung bei Patienten mit AHF erfolgt prinzipiell ähnlich wie bei anderen Patienten pharmakologisch, katheterinterventionell mittels Ablationsverfahren bzw. durch Schrittmacher- oder Defibrillator-Implantation [23, 24]. Alle diese therapeutischen Ansätze sind allerdings schwieriger als bei Patienten ohne AHF.
Pulmonale Hypertonie
Eine pulmonalarterielle oder pulmonale Hypertonie (P(A)H-AHF) entwickelt sich insbesondere bei primären Links-rechts-Shuntvitien, angeborenen Obstruktionen des linken Herzens, zyanotischen Herzfehlern mit vermehrtem Lungenfluss sowie Anomalien der Pulmonalarterien [25-27].
Für eine spezifische Pharmakotherapie, die zu einer Verbesserung der Lebensqualität und der Prognose führen kann, stehen auch bei der P(A)H-AHF die typischen PAH-spezifischen Medikamente (Endothelin-Antagonisten, PDE-5-Inhibitoren, sGC-Stimulatoren, Prostanoide, IP-Prostazyklin-Rezeptor-Agonisten) zur Verfügung [28-30]. Da sich die P(A)H-AHF von anderen PAH-Formen unterscheidet, sollten diese Patienten stets gemeinsam mit EMAH-Spezialisten geführt werden, insbesondere hinsichtlich einer PAH-spezifischen Therapie, einer operativen oder interventionellen Behandlung oder bei Entscheidungen bis hin zur Herz-Lungen-Transplantation [28, 30-32].
Infektiöse Endokarditis
Die Häufigkeit einer infektiösen Endokarditis liegt bei EMAH höher als in der Allgemeinbevölkerung [33-45]. Besonders hoch ist das Risiko bei komplexen AHF, Ventrikelseptumdefekten, Herzklappenprothesen und linksseitiger Herzerkrankung [34, 44].
Gerade bei AHF sollten beim klinischen Verdacht auf eine infektiöse Endokarditis, bei anhaltendem Fieber, Nachtschweiß, unklarem Gewichtsverlust oder neu aufgetretener Herzinsuffizienz frühzeitig entsprechende diagnostische Schritte eingeleitet werden, idealerweise VOR Beginn einer Antibio-tikatherapie.
Wegen der immer noch hohen Letalität der Erkrankung sollten gefährdete Patienten eine effektive Endokarditisprophylaxe erhalten. Die aktuelle ESC-Leitlinie empfiehlt eine Endokarditisprophylaxe nur noch für Hochrisikopatienten mit einem zu erwartenden schweren Verlauf [45, 46]. Gerade bei AHF werden aber die neuen Empfehlungen durchaus kontrovers diskutiert und es wird teilweise ein breiteres Indikationsspektrum gesehen. Sicher ist es wichtig, in das geforderte Endokarditis-Team einen EMAH-Kardiologen zu integrieren.
Erworbene Komorbiditäten
Zusätzlich zu den erwähnten herzfehlerspezifischen Komplikationen aggravieren erworbene Komorbiditäten den Langzeitverlauf von AHF oder ihre Ausprägung selbst wird durch den zugrundeliegenden AHF beeinflusst [47, 48]. Hierzu gehören u. a. die koronare Herzerkrankung, die arterielle Hypertonie, Stoffwechselstörungen (Diabetes mellitus, Hyperlipidämie, metabolisches Syndrom), zerebrovaskuläre Erkrankungen oder Organschäden, insbesondere an Leber und Nieren. Hier bekommen präventivmedizinische Maßnahmen, auch durch den Hausarzt, künftig immer mehr Bedeutung, wobei allerdings ebenfalls vitientypische Besonderheiten zu berücksichtigen sind.
Psychische Erkrankungen
Bis heute noch wenig Aufmerksamkeit erhalten psychische Erkrankungen. Hier sind posttraumatische Belastungsstörungen, Depressionen und Angststörungen zu nennen [47, 48, 50-52]. Obwohl EMAH insgesamt eine gute allgemeine Lebensqualität zugeschrieben wird, ist die gesundheitsbezogene Lebensqualität im Vergleich zu gesunden Erwachsenen reduziert [53-56]. Wahrscheinlich sind EMAH einer konstanten, psychischen Belastung ausgesetzt, die sich negativ auf den Krankheitsverlauf auswirken kann, bis hin zu vorzeitiger Sterblichkeit [57].
Auch eine mögliche Medikation bei psychischen Erkrankungen von EMAH bedarf besonderer Überlegungen. Daher ist es notwendig, zusammen mit dem Hausarzt die psychosoziale Versorgung von EMAH auszubauen.
Ko-Autoren: Stephan Achenbach, Caroline Andonian, Jürgen Beckmann, Fokko de Haan, Gerhard-Paul Diller, Peter Ewert, Sebastian Freilinger, Ulrike Gundlach, Michael Huntgeburth, Dirk Loßnitzer, Nicole Nagdyman, Lars Pieper, Jörg Schelling, Michael Weyand und Rhoia Neidenbach
Mögliche Interessenkonflikte: Die Autoren haben keine deklariert.
Literatur
- Neidenbach R, Kaemmerer H, Pieper L, Ewert P, Schelling J. [Striking Supply Gap in Adults with Congenital Heart Disease?]. Dtsch Med Wochenschr. 2017;142(4):301-3.
- Deutsche Herzstiftung e.V. Deutscher Herzbericht 2018. Frankfurt Deutsche Herzstiftung e.V. ; 2018.
- Neidenbach R, Pieper L, Freilinger S, Nebel K, Sanftenberg L, Schelling J, et al. Adults with congenital heart disease: lack of specific disease related medical health care from the patients point of view. European Heart Journal. 2018;39:111.
- Neidenbach R, Pieper L, Sanftenberg L, Schelling J, Freilinger S, Seidel L, et al. Adults with congenital heart disease: lack of specific disease related medical health care from the general practitioners view. European Heart Journal. 2018;39:112.
- Perloff JK, Warnes CA. Challenges posed by adults with repaired congenital heart disease. Circulation. 2001;103(21):2637-43.
- Stout KK, Daniels CJ, Aboulhosn JA, Bozkurt B, Broberg CS, Colman JM, et al. 2018 AHA/ACC Guideline for the Management of Adults With Congenital Heart Disease: Executive Summary. Circulation. 2018:CIR0000000000000602.
- Piran S, Veldtman G, Siu S, Webb GD, Liu PP. Heart failure and ventricular dysfunction in patients with single or systemic right ventricles. Circulation. 2002;105(10):1189-94.
- Faccini A, Micheletti A, Negura D, Giugno L, Butera G, Carminati M, et al. Heart failure in grown-up congenital heart disease. Minerva cardioangiologica. 2018.
- Lal S, Kotchetkova I, Cao J, Jackson D, Cordina R, Celermajer DS. Heart failure admissions and poor subsequent outcomes in adults with congenital heart disease. European journal of heart failure. 2017.
- Neidenbach R, Niwa K, Oto O, Oechslin E, Aboulhosn J, Celermajer D, et al. Improving medical care and prevention in adults with congenital heart disease-reflections on a global problem-part I: development of congenital cardiology, epidemiology, clinical aspects, heart failure, cardiac arrhythmia. Cardiovasc Diagn Ther. 2018;8(6):705-15.
- Budts W, Roos-Hesselink J, Radle-Hurst T, Eicken A, McDonagh TA, Lambrinou E, et al. Treatment of heart failure in adult congenital heart disease: a position paper of the Working Group of Grown-Up Congenital Heart Disease and the Heart Failure Association of the European Society of Cardiology. Eur Heart J. 2016;37(18):1419-27.
- Brida M, Diller G-P, Gatzoulis MA. Systemic Right Ventricle in Adults With Congenital Heart Disease: Anatomic and Phenotypic Spectrum and Current Approach to Management. Circulation. 2018;137(5):508-18.
- Therrien J, Provost Y, Harrison J, Connelly M, Kaemmerer H, Webb GD. Effect of angiotensin receptor blockade on systemic right ventricular function and size: a small, randomized, placebo-controlled study. Int J Cardiol. 2008;129(2):187-92.
- van der Bom T, Winter MM, Bouma BJ, Groenink M, Vliegen HW, Pieper PG, et al. Effect of valsartan on systemic right ventricular function: a double-blind, randomized, placebo-controlled pilot trial. Circulation. 2013;127(3):322-30.
- Hechter SJ, Fredriksen PM, Liu P, Veldtman G, Merchant N, Freeman M, et al. Angiotensin-converting enzyme inhibitors in adults after the Mustard procedure. Am J Cardiol. 2001;87(5):660-3, A11.
- Robinson B, Heise C, Moore J, Anella J, Sokoloski M, Eshaghpour E. Afterload reduction therapy in patients following intraatrial baffle operation for transposition of the great arteries. Pediatric cardiology. 2002;23(6):618-23.
- Lester SJ, McElhinney DB, Viloria E, Reddy GP, Ryan E, Tworetzky W, et al. Effects of losartan in patients with a systemically functioning morphologic right ventricle after atrial repair of transposition of the great arteries. Am J Cardiol. 2001;88(11):1314-6.
- Dore A, Houde C, Chan KL, Ducharme A, Khairy P, Juneau M, et al. Angiotensin receptor blockade and exercise capacity in adults with systemic right ventricles: a multicenter, randomized, placebo-controlled clinical trial. Circulation. 2005;112(16):2411-6.
- Oechslin EN, Harrison DA, Connelly MS, Webb GD, Siu SC. Mode of death in adults with congenital heart disease. Am J Cardiol. 2000;86(10):1111-6.
- Nieminen HP, Jokinen EV, Sairanen HI. Causes of late deaths after pediatric cardiac surgery: a population-based study. J Am Coll Cardiol. 2007;50(13):1263-71.
- Warnes CA, Williams RG, Bashore TM, Child JS, Connolly HM, Dearani JA, et al. ACC/AHA 2008 guidelines for the management of adults with congenital heart disease. Circulation. 2008;118(23):e714-e833.
- Moore B, Yu C, Kotchetkova I, Cordina R, Celermajer DS. Incidence and clinical characteristics of sudden cardiac death in adult congenital heart disease. International journal of cardiology. 2017.
- Hernandez-Madrid A, Paul T, Abrams D, Aziz PF, Blom NA, Chen J, et al. Arrhythmias in congenital heart disease: a position paper of the European Heart Rhythm Association (EHRA), Association for European Paediatric and Congenital Cardiology (AEPC), and the European Society of Cardiology (ESC) Working Group on Grown-up Congenital heart disease, endorsed by HRS, PACES, APHRS, and SOLAECE. Europace. 2018.
- Khairy P, Van Hare GF, Balaji S, Berul CI, Cecchin F, Cohen MI, et al. PACES/HRS expert consensus statement on the recognition and management of arrhythmias in adult congenital heart disease: developed in partnership between the Pediatric and Congenital Electrophysiology Society (PACES) and the Heart Rhythm Society (HRS). Endorsed by the governing bodies of PACES, HRS, the American College of Cardiology (ACC), the American Heart Association (AHA), the European Heart Rhythm Association (EHRA), the Canadian Heart Rhythm Society (CHRS), and the International Society for Adult Congenital Heart Disease (ISACHD). Can J Cardiol. 2014;30(10):e1-e63.
- Diller GP, Gatzoulis MA. Pulmonary vascular disease in adults with congenital heart disease. Circulation. 2007;115(8):1039-50.
- Duffels MG, Engelfriet PM, Berger RM, van Loon RL, Hoendermis E, Vriend JW, et al. Pulmonary arterial hypertension in congenital heart disease: an epidemiologic perspective from a Dutch registry. Int J Cardiol. 2007;120(2):198-204.
- Hjortshøj CS, Jensen AS, Sørensen K, Nagy E, Johansson B, Kronvall T, et al. Epidemiological changes in Eisenmenger syndrome in the Nordic region in 1977–2012. Heart. 2017;103(17):1353-8.
- Kaemmerer H, Apitz C, Brockmeier K, Eicken A, Gorenflo M, Hager A, et al. Pulmonary hypertension in adults with congenital heart disease: Updated recommendations from the Cologne Consensus Conference 2018. Int J Cardiol. 2018;272S:79-88.
- Hoeper MM, Apitz C, Grunig E, Halank M, Ewert R, Kaemmerer H, et al. Targeted therapy of pulmonary arterial hypertension: Updated recommendations from the Cologne Consensus Conference 2018. Int J Cardiol. 2018;272S:37-45.
- Galie N, Humbert M, Vachiery JL, Gibbs S, Lang I, Torbicki A, et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension: The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS): Endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC), International Society for Heart and Lung Transplantation (ISHLT). Eur Heart J. 2016;37(1):67-119.
- Brida M, Gatzoulis MA. Pulmonary arterial hypertension in adult congenital heart disease. Heart. 2018:heartjnl-2017-312106.
- D’Alto M, Diller GP. Pulmonary hypertension in adults with congenital heart disease and Eisenmenger syndrome: current advanced management strategies. Heart. 2014;100(17):1322-8.
- Montanaro C, Dimopoulos K, Shore DF. Infective endocarditis in patients with congenital heart disease: When, where and how. International Journal of Cardiology. 2017;249:171-2.
- Moore B, Cao J, Kotchetkova I, Celermajer DS. Incidence, predictors and outcomes of infective endocarditis in a contemporary adult congenital heart disease population. Int J Cardiol. 2017;249:161-5.
- Berglund E, Johansson B, Dellborg M, Sorensson P, Christersson C, Nielsen NE, et al. High incidence of infective endocarditis in adults with congenital ventricular septal defect. Heart. 2016.
- Baddour LM, Wilson WR, Bayer AS, Fowler VG, Tleyjeh IM, Rybak MJ, et al. Infective endocarditis in adults: diagnosis, antimicrobial therapy, and management of complications: a scientific statement for healthcare professionals from the American Heart Association. Circulation. 2015;132(15):1435-86.
- Correa de Sa DD, Tleyjeh IM, Anavekar NS, Schultz JC, Thomas JM, Lahr BD, et al. Epidemiological trends of infective endocarditis: a population-based study in Olmsted County, Minnesota. Mayo Clin Proc. 2010;85(5):422-6.
- Duval X, Delahaye F, Alla F, Tattevin P, Obadia J-F, Le Moing V, et al. Temporal trends in infective endocarditis in the context of prophylaxis guideline modifications: three successive population-based surveys. Journal of the American College of Cardiology. 2012;59(22):1968-76.
- Federspiel JJ, Stearns SC, Peppercorn AF, Chu VH, Fowler VG. Increasing US rates of endocarditis with Staphylococcus aureus: 1999-2008. Archives of internal medicine. 2012;172(4):363-5.
- Abdulhak AAB, Baddour LM, Erwin PJ, Hoen B, Chu VH, Mensah GA, et al. Global and regional burden of infective endocarditis, 1990–2010: a systematic review of the literature. Global heart. 2014;9(1):131-43.
- Cresti A, Chiavarelli M, Scalese M, Nencioni C, Valentini S, Guerrini F, et al. Epidemiological and mortality trends in infective endocarditis, a 17-year population-based prospective study. Cardiovasc Diagn Ther. 2017;7(1):27-35.
- Murdoch DR, Corey GR, Hoen B, Miró JM, Fowler VG, Bayer AS, et al. Clinical presentation, etiology, and outcome of infective endocarditis in the 21st century: the International Collaboration on Endocarditis–Prospective Cohort Study. Archives of internal medicine. 2009;169(5):463-73.
- Tleyjeh IM, Abdel-Latif A, Rahbi H, Scott CG, Bailey KR, Steckelberg JM, et al. A systematic review of population-based studies of infective endocarditis. Chest. 2007;132(3):1025-35.
- Kuijpers JM, Koolbergen DR, Groenink M, Peels KC, Reichert CL, Post MC, et al. Incidence, risk factors, and predictors of infective endocarditis in adult congenital heart disease: focus on the use of prosthetic material. European heart journal. 2017;38(26):2048-56.
- Naber C, B. Al-Nawas, H. Baumgartner, H.-J. Becker, M. Block, R. Erbel, , G. Ertl UF, D. Franzen, C. Gohlke-Bärwolf, R. Gattringer, W. Graninger, , W. Handrick MH, R. Heying, D. Horstkotte, A. Jaussi, P. Kern, H.-H. Kramer, S. Kühl, P. M. Lepper, R. G. Leyh, H. Lode, U. Mehlhorn, P. Moreillon, A. Mügge, , R. Mutters JN, G. Peters, R. Rosenhek, A. A. Schmaltz, H. Seifert, P. M. Shah, H. Sitter, W. Wagner, G. Wahl, K. Werdan, M. Zuber. Prophylaxe der infektiösen Endokarditis. Kardiologe. 2007;1:243–50.
- Habib G, Lancellotti P, Antunes MJ, Bongiorni MG, Casalta JP, Del Zotti F, et al. 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by: European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM). European heart journal. 2015;36(44):3075-128.
- Neidenbach RC, Lummert E, Vigl M, Zachoval R, Fischereder M, Engelhardt A, et al. Non-cardiac comorbidities in adults with inherited and congenital heart disease: report from a single center experience of more than 800 consecutive patients. Cardiovasc Diagn Ther. 2018;8(4):423-31.
- Singh S, Desai R, Fong HK, Sadolikar A, Samani S, Goyal H. Extra-cardiac comorbidities or complications in adults with congenital heart disease: a nationwide inpatient experience in the United States. Cardiovasc Diagn Ther. 2018;8(6):814-9.
- Grunig E, Benjamin N, Kruger U, Kaemmerer H, Harutyunova S, Olsson KM, et al. General measures and supportive therapy for pulmonary arterial hypertension: Updated recommendations from the Cologne Consensus Conference 2018. Int J Cardiol. 2018;272S:30-6.
- Andonian C, Beckmann J, Biber S, Ewert P, Freilinger S, Kaemmerer H, et al. Current research status on the psychological situation of adults with congenital heart disease. Cardiovasc Diagn Ther. 2018;8(6):799-804.
- Jackson JL, Leslie CE, Hondorp SN. Depressive and Anxiety Symptoms in Adult Congenital Heart Disease: Prevalence, Health Impact and Treatment. Prog Cardiovasc Dis. 2018;61(3-4):294-9.
- Westhoff-Bleck M, Briest J, Fraccarollo D, Hilfiker-Kleiner D, Winter L, Maske U, et al. Mental disorders in adults with congenital heart disease: Unmet needs and impact on quality of life. J Affect Disord. 2016;204:180-6.
- Lane DA, Lip GY, Millane TA. Quality of life in adults with congenital heart disease. Heart. 2002;88(1):71-5.
- Moons P, Van Deyk K, Marquet K, Raes E, De Bleser L, Budts W, et al. Individual quality of life in adults with congenital heart disease: a paradigm shift. Eur Heart J. 2005;26(3):298-307.
- Apers S, Kovacs AH, Luyckx K, Thomet C, Budts W, Enomoto J, et al. Quality of Life of Adults With Congenital Heart Disease in 15 Countries: Evaluating Country-Specific Characteristics. J Am Coll Cardiol. 2016;67(19):2237-45.
- Eslami B, Sundin O, Macassa G, Khankeh HR, Soares JJ. Anxiety, depressive and somatic symptoms in adults with congenital heart disease. J Psychosom Res. 2013;74(1):49-56.
- Watkins LL, Koch GG, Sherwood A, Blumenthal JA, Davidson JR, O’Connor C, et al. Association of anxiety and depression with all-cause mortality in individuals with coronary heart disease. J Am Heart Assoc. 2013;2(2):e000068.
- Lesch W, Specht K, Lux A, Frey M, Utens E, Bauer U. Disease-specific knowledge and information preferences of young patients with congenital heart disease. Cardiol Young. 2014;24(2):321-30.
- Diller GP, Breithardt G, Baumgartner H. Congenital heart defects in adulthood. Dtsch Arztebl Int. 2011;108(26):452-9.
Danksagung: Die Autoren danken der “Deutschen Herzstiftung” und “Herzkind e. V., sowie den Firmen “Actelion Pharmaceuticals Deutschland GmbH”, “Nambaya” und “Data input” für die Unterstützung der Versorgungsforschung bei Erwachsenen mit angeborenen Herzfehlern für die gewährte, nicht zweckgebundene Forschungszuwendung (unrestricted educational grant). Ganz besonderer Dank an die Deutsche Herzstiftung, die uns die Genehmigung zur Verwendung der Abbildungen gegeben hat.

